Страница: 7/8
4.2 Роль отдельных группировок в молекуле тиамина для его связывания в тканях.
За последние годы синтезировано более десятка новых производных тиамина (смешанные дисульфиды, О-бензольные производные и др.), широко внедряемых в лечебную и профилактическую практику. Преимущества новых витаминных препаратов, как правило, выявлялись чисто эмпирически в связи с тем, что до настоящего времени мы не располагаем достаточными сведениями о молекулярных механизмах ассимиляции тиамина, о характере его взаимодействия со специфическими (ферменты) и неспецифическими (осуществляющими транспорт витамина) белками. Необходимость точных представлений в этом вопросе диктуется и широкими перспективами использования антивитаминов тиамина (ампрол, хлоротиамин, деокситиамин) для лечебных целей (см. ниже).
Работы по синтезу новых производных тиамина с заранее заданными физико-химическими свойствами, обусловливающими возможности целенаправленного воздействия на обменные процессы в организме, немыслимы без конкретных представлений о роли отдельных групп атомов витамина и его производных в этой области. Значение пирофосфатного радикала для специфической потеидизации ТДФ в составе соответствующих ферментов уже отмечалось выше. В последние годы становится все более очевидным участие тиамина в других реакциях, не имеющих ничего общего с коферменными функциями витамина. Разнообразию активных группировок в молекуле тиамина соответствует каждый раз особая форма- претеидизации, блокирующая одни и обнажающая одновременно другие, важные для соответствующей функции, участки молекулы витамина (Ю. М. Островский, 1971). Действительно, первый тип протеидизации (через пирофосфатный радикал) отвечает коферментной функции и оставляет свободными, доступными для субстрата 2-й углерод тиазола и аминогруппу пиримидинового компонента. С другой стороны, очевидно, что участие витамина в окислительно-восстановительных реакциях или в процессах перефосфорилирования должно сочетаться с исключением возможности одновременного функционирования его как кофермента, так как в первом случае необходима деполяризация и раскрытие тиазолового цикла, а во втором — свободное положение фосфорилированного оксиэтильного радикала. Поскольку 80—90% тиамина, присутствующего в тканях, освобождается лишь при кислотном и ферментативном гидролизе, можно считать, что все связанные формы витамина находятся в протеидизированном, т. е. связанном с белками, состоянии.
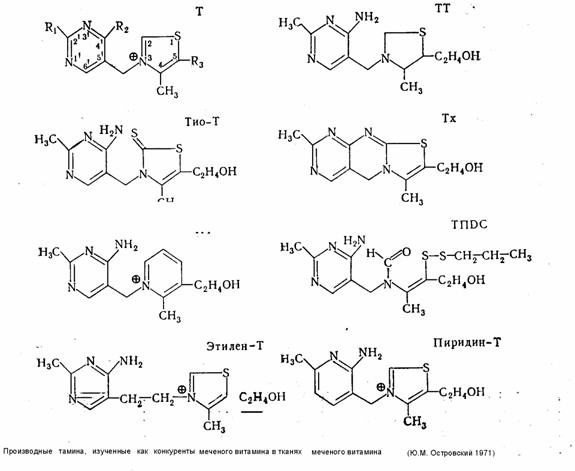
Представление о значении отдельных участков молекулы тиамина в этом процессе легко получить, определяя степень связывания тканями меченного по сере (S35) витамина и некоторых его производных, лишенных тех или иных активных центров, например аминогруппы — окситиамин (окси-Т), аминогруппы и оксиэтильного радикала — хлорокситиамин (ХОТ), четвертичного азота в тиазоловом цикле тетрагидротиамин (TТ) Некоторые ограничения на интерпретацию данных, полученных таким образом в короткие сроки опыта, накладывают физиологические механизмы, транспорта и экскреции вводимых соединений, в связи с чем дополнительно приходится исследовать также выведение витамина и самих меченых соединений с мочой. С другой стороны, результаты, получаемые в длительные сроки (24 часа), почти полностью соответствуют только представлениям о протеидизированной части витамина, а на основании рассмотрения конкурентных взаимоотношений между различными упомянутыми выше мечеными и другими немечеными производными витамина можно последовательно исключать роль отдельных атомов или группировок в механизмах фиксации тиамина тканями.
4.3 Коферментные функции тиаминдифосфата.
Известно значительное количество различных реакций, катализируемых ТДФ. Однако все их можно свести к нескольким типичным вариантам: простое и окислительное декарбоксидирование a-кетокислот, ацилоиновая конденсация, фосфорокластическое расщепление кетосахаров. Ферментные системы, принимающие участие в этих реакциях по-видимому, едины в основных принципах своего действия; различна лишь последующая судьба «активного альдегидного осколка», возникающего на первых этапах процесса. Успехи, достигнутые в течение последних лет в изучении превращений a-кетокислот (С. Е. Северин, 1964; А. А. Глемжа, 1964), позволили четко представить как роль собственно декарбоксилирующего фрагмента полиферментного комплекса дегидрогеназы, содержащего ТДФ, так и последовательность всех других, связанных с ним реакций:
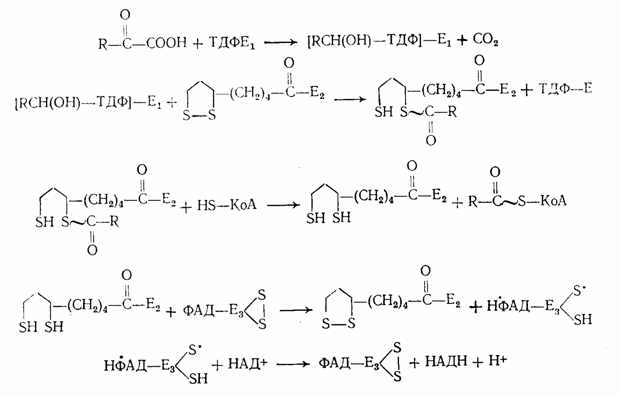
В системе транскетолазы (ТК) «активный альдегидный» осколок, очевидно, будет представлен гликолевым радикалом, переносимым от соответствующих источников (ксилулозо-5-фосфат, фруктозо-6-фосфат, оксипируват и др.) на различные акцепторы (рибозо-5-фосфат, эритро-зо-4-фосфат, глюкозо-6-фосфат). В фосфокетолазной реакции «активный гликолевый» радикал превращается непосредственно в ацетилфосфат.
Значительные успехи в выяснении механизма каталитического действия ТДФ были достигнуты в результате исследований, проведенных в двух основных направлениях: создание модельных неферментативных систем и введение в ферментные системы различных аналогов или антагонистов тиамина. Используя первый путь, удалось показать, что витамин и в нефосфорилированном виде способен при определенных условиях в отсутствие белка катализировать реакции декарбоксилирования, образования ацетона, дисмутации диацетила. Различными вариантами опытов, в которых коферментная активность ТДФ сравнивалась с активностью антиметаболитов витамина или изучалась с добавлением соли Рейнеке, бромацетата, пара-хлор-ртуть-бензоата и других соединений, показано, что каталитически наиболее важными группами в молекуле тиамина являются: сера, четвертичный азот тиазолового кольца, аминогруппа в положении 4 пиримидинового: кольца, второй углеродный атом тиазола (2-С-Тз), метиленовый мостик. Можно считать устоявшимся представление, что часть перечисленных выше активных центров (сера, азот, метиленовый мостик) крайне необходима только для поддержания определенной структуры и создания соответствующей электронной плот-ности-(Б. Пюльман, А. Пюльман, 1965) у второго углеродного атома тиазола (2-С-Тз), который является главным каталитическим центром. Спорными и неопределенными пока являются представления о значении аминогруппы пиримидинового компонента.
Некоферментная активность тиамина и некоторых его производных.
За последние 20 лет наряду выяснением механизма основных реакций, в которых каталитическую роль играет ТДФ, стали накапливаться данные о высокой биологической активности других некоферментных производных тиамина. Отчетливо наметились два направления исследований: возможное, участие различных фосфорных эфиров витамина в активном переносе богатых энергией фосфатных групп (ангидридная связь в ТДФ макроэргическая) и вероятность вмешательства тиамина в окислительно-восстановительные реакции В связи с тем что неизвестны специфические тиаминсодержащие ферментные системы, причастные к регуляции упомянутых выше процессов, наблюдаемые в этой сфере обмена эффекты витамина можно рассматривать как проявление его неспецифических функций.
Тиаминофосфаты (ТФ).
После разработки доступных методов получения ТДФ последний стали широко испытывать при различных заболеваниях в клинических условиях. Внутривенное введение 100—500 мг ТДФ при диабетическом ацидозе увеличивало количество пирувата, образующегося из глюкозы. Эффект аналогичного характера наблюдался при диабете после введения АТФ или фосфокреатина. Инкубация цельной крови с Р32н в присутствии Зх10-3М тиамина сопровождалась ускоренным внедрением метки в промежуточные продукты гликолиза (фруктозо-1,6-дифосфат, фруктозо-6-фосфат). Особенно заметно во времени, по сравнению с контролем без витамина, возрастала радиоактивность триозофосфатов. По данным Л. Н. Кузнецовой, Е. В. Лахно и Р. В. Чаговец (1953), в мышцах при утомлении и отдыхе распад и ресинтез ТДФ происходят примерно по тем же закономерностям, которые известны для АТФ и фосфокреатина. Характерными были изменения во время отдыха, когда количество ТДФ превышало исходный уровень до утомительной работы. Авторы не рассматривают причин усиленного распада ТДФ во время сократительной деятельности мышц, и вряд ли это возможно с позиции известных коферментных функций ТДФ. Торможение функциональной активности печени (введение ССЦ, гипоксия), по-видимому, за счет снижения расхода, сопровождается накоплением в органе ТФ. Наконец, совместное с глюкозой скармливание больших количеств ТДФ крысам сопровождалось заметным (на 69%) повышением уровня АТФ в печени.
Группа японских исследователей подробно изучила на циклофоразной системе внедрение Р32 из меченого ТДФ в немеченый АТФ. Перенос метки был в 3—4 раза больше в присутствии Р32-ТДФ, чем в присутствии неорганического Р32н, хотя система и во втором случае содержала столько же ТДФ. Если циклофоразную систему выделяли из печени страдающих от недостаточности тиамина крыс, то внедрение Р32 в АТФ из меченого ТДФ превышало контроль в 8—10 раз. Независимость внедрения Р32 в АТФ от эстерификации неорганического фосфата подтверждалась и тем, что ДНФ (10-4М), снижавший интенсивность окислительного фосфорилирования в 5—10 раз, не влиял на процесс переноса метки от ТДФ к АТФ.
Еще более интересными представляются результаты сравнительного изучения физико-химической и «субстратной» разнозначности концевых фосфатов АТФ и ТТФ. Оба соединения одинаково гидролизуются картофельной апиразой и кристаллическими препаратами миозина. Макроэргический характер фосфатных остатков в ТФ побудил ряд авторов исследовать роль этих соединений в начальных реакциях углеводного обмена. Пекарские дрожжи (Kiessling, 1957) в присутствии Р32н, и глюкозы интенсивно накапливают метку вначале преимущественно в g-фосфате ТТФ и АТФ, а затем в α- и β-фосфатах. Удельная активность ТТФ в определенных условиях опыта может уравниваться с таковой для АТФ, что рассматривается как выражение причастности ТФ к переносу лабильных фосфатов при обмене глюкозы. Действительно, на белковых препаратах из дрожжей g-Р32 ТТФ переносится на глюкозу в присутствии АДФ. Смесь ТФ (около 70% ТТФ), неактивная сама по себе, в присутствии АТФ стимулирует потребление глюкозы гексокиназой, полученной из миокарда, но не из скелетных мышц. Митохондрии содержат значительные количества ТФ, которые могут быть удалены на ¾ без заметного нарушения окисления ПК или сукцината. Сами эти ТФ захватывают до 75% Р32н по отношению к АТФ, а классический разобщающий яд ДНФ тормозит образование АТФ в большей степени, чем ТФ. Введение животным окси-Т, в зависимости от характера субстратов дыхания, может нарушать в митохондриях отдельно окислительные и фосфорилирующие реакции, а на интактных митохондриях, инкубируемых в отсутствие АТФ, добавление ТФ (особенно ТМФ) достоверно повышает эстерификацию неорганического фосфата. В последнее время установлено, что введение животным больших доз ТДФ уже через несколько часов значительно, (иногда в 2 раза) повышает в тканях содержание лабильных фосфорных соединений. Интересной представляется заметно большая эффективность ТМФ в ряде опытов, что, возможно, связано со своеобразным отношением этого производного тиамина к мембранам или обусловлено более легким его превращением в ТТФ. Есть основания полагать, что имеются определенные особенности взаимодействия ТФ с фосфорилирующими реакциями в различных тканях. В нервной ткани, например, с превращением ТФ ряд авторов связывают физиологические акты проведения возбуждения (Muralt, 1962) и транспорт ионов натрия через мембраны.
Реферат опубликован: 15/06/2005 (16952 прочтено)